2021-2022 英语周报 八年级 新目标 5 AHW答案

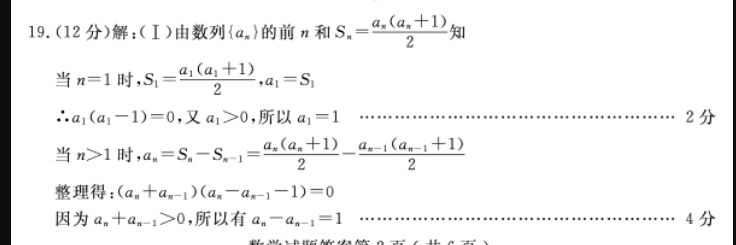

19.(12分)解:(1)由数列{a,)的前n和S,=9.(a1+1知当n=1时,s1=a1(a+1,a1=S∴a1(a1-1)=0,又a1>0,所以a1=1……分当n>1时,an=S。-S-1≈9(an+1)_an-1(an-1+1)整理得:(an+an-1)(an-an-1-1)=0因为an+an1>0,所以有an-an1=1分所以数列{an}是首项a1=1,公差d=1的等差数列数列{an}的通项公式为an=a1+(n-1)d=n………………………………6分(Ⅱ)由an=n知:bn=log数列{b}的前n项和为h+b+b+…+b=1og22+log:3+lg+…+lgnog2(2×3×x…x×n+1)=1og2(n+2)-1……………………………8分令b十b2+b2+…十b。=k(k∈Z则有log2(n+2)-1=k,n=2*+1-2由n∈(0,2020),k∈Z知,k<10且k∈N10分所以区间(0,2020)内所有“优化数”的和为S=(22-2)+(23-2)+(24-2)+…+(210-2)=(22+23+24+2)-18-22(1-2)-18=21-22=2026…………………12分


27.(14分)(1)Mg: B, Os. H2O+2H2SO,-2H3 BO3+2MgSO4(2分提高反应温度、减小铁硼矿粉粒径(1分)(2)Fe3O4(1分)SiO2和CaSO4(2分)(3)将Fe2+氧化成Fe3+(1分)使Fe2+与A3+形成氢氧化物沉淀而除去(1分)(4)(七水)硫酸镁(2分)HNa"[H: B: H](5)H(2分)(6)2H3BO3=B2O3+3H2O;B2O3+3Mg3MgO+2B(写2HBO3+3Mg4-3Mg0+2B+3H2O也给分)(2分)【解析】(1)Mg2B2O3·H2O与硫酸反应属于强酸制备弱酸过程,反应的化学方程式为Mg2B2O3·H2O+2H2SO2MgSO,+2H3BO3。为提高浸出速率,可以增大其接触面积(如研细粉末)或者升高温度。(2)Fe2O4俗称磁性氧化铁,可以利用它的磁性将其从“浸渣”中分离。由于SO2不溶于三大强酸,所以“浸渣”中还剩余的物质是SiO2及生成的CaSO4。(3)H2O2溶液是“绿色”氧化剂,其作用是氧化溶液中的Fe+;根据流程,调节溶液的pH约为5,主要目的是除去溶液中的AP和Fe+,使它们生成沉淀而除去。(4)根据流程图,MgSO4或其水合物会混杂在“粗硼酸中。(5)在NaBH4中BH7是原子团,其中HHNa(H: B: H]-显-1价,其电子式为H(6)以硼酸和金属镁为原料可制备单质硼,分两步,先是H2BO3受热分解:2H3BO3=B2O3+3H2O然后是Mg置换B:B2O3+3Mg=3MgO+2B。

以上就是2021-2022 英语周报 八年级 新目标 5 AHW答案,更多英语周报答案请关注本网站。






