英语周报2021-2022九年级外研第19期答案


27.(1)物理变化(1分)(2)不能(1分);zrSO难溶于盐酸,后续依然需要用氯气和石油焦与锆英石反应,浪费药品(2分)(3)ZrSO4+4Cl2+4C=ZrCl4+SiCl4+4CO(写“ZnSO4+4Cl2+2C=ZrCl4+SiCl4+2CO2”也给分,2分)(4)取少许最后一次的洗涤液于试管中,加入适量硝酸酸化的AgNO3溶液,若无沉淀产生,则已洗涤干净(或其他合理答案,2分)(5)2C1-2e=Cl2↑(2分);9.1g(2分)(6)7.7(2分)【解析】本题主要考査制备海绵锆的工艺流程,考查学生对元素化合物的理解能力和综合运用能力。(2)硅酸盐难溶于酸,不能用盐酸来溶解锆英石。(5)阴极的反应式为ZrF3+4e—Zr+6F,每转移0.4mole,生成0. 1 mol zr,故阴极增重9.1g。(6)在Zr(CO2)2饱和溶液中:Zr(CO3)2、Zr4++2CO),设电离出的c(Zr1+)=amol·L-1,c(CO-)=2amol·L1,K[Zr(CO3)2]=c(Zr4)·c2(CO)=4a3=4.0×10-12,a=104,pc(Zr4+)=4,pc(CO))=3.7,pc(Zr+)+pc(CO))=7.7。
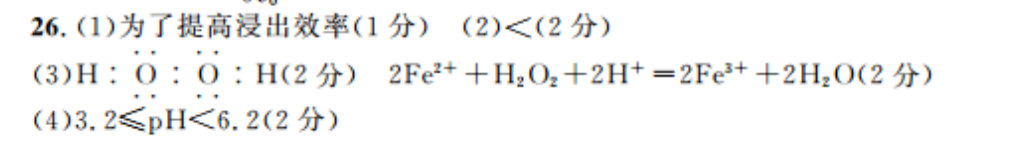

26.(1)为了提高浸出效率(1分)(2)<(2分)(3)H:O:O:H(2分)2Fe2++H2O2+2H+=2Fe3++2H2O(2分)(4)3.2≤pH<6.2(2分)(5)2Zn2'++HCO +3NH3.H,O=Zng (OH)2 CO3+3NH* +H2 O(2 23)(6)2Fe(OH)3+3C10+40H--2Fe0X-+3CI-+5H, O(2 3) Fe0:-+3e+4H, OFe(OH)3+5OH-(2分)(1)堆浸时将氧化铜锌矿粉碎的目的是为了提高浸出效率;(2)硫化铜不溶解,硫化锌溶解说明K(CuS)小于K(ZnS);(3)H2O2是共价化合物,电子式是H:O:O:H,加入H2O2氧化Fe2+,离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O;(4)由题中金属离子沉淀的pH,使Zn2+不沉淀,而Fe3+完全沉淀的PH是3.2≤pH<6.2;(5)加入碳酸氢铵和氨水发生反应生成Zn2(OH)2CO2的离子方程式是2Zn2++HCO3+3NH3,H2O=Zn2(OH)2CO3+3NH+H2O;(6)Fe(OH)3可用KClO溶液在碱性环境下将其氧化得到一种高效的多功能水处理剂一K2FeO4由氧化还原反应规律知,发生反应的离子方程式是2Fe(OH)3+3ClO-+4OH-一2FeO-+3Cl-+5H2O,高铁电池负极反应是Zn-2e-+20H=Zn(OH)2,正极反应式是FeO-+3e-+4H2O=Fe(OH)3+5OH-。]

以上就是英语周报2021-2022九年级外研第19期答案,更多英语周报答案请关注本网站。






