2022九年级英语周报新目标人教版第五期答案

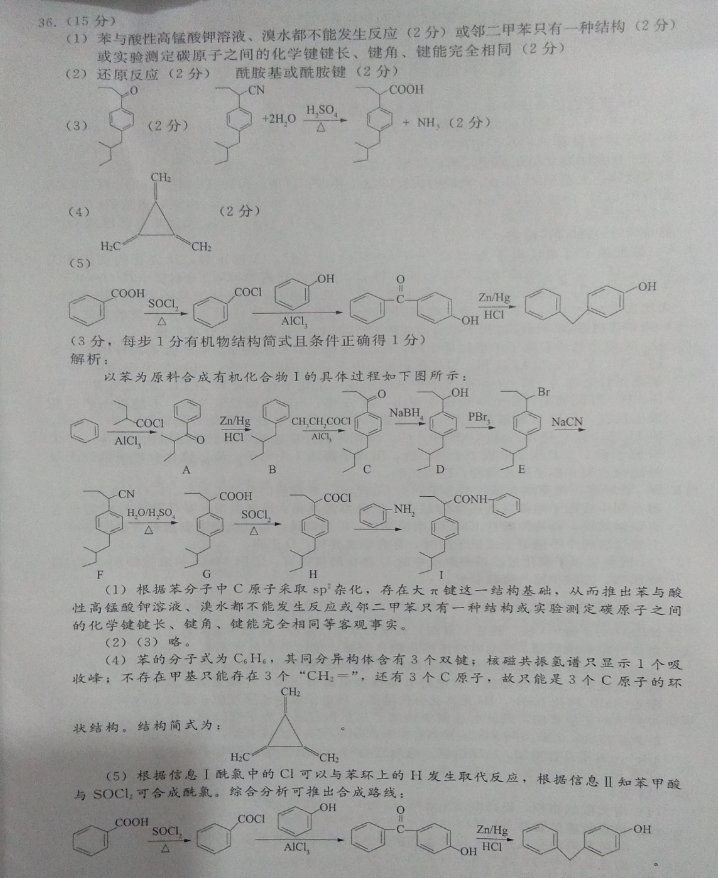
36.(15分)(1)苯与酸性高锰酸钾溶液、溴水都不能发生反应(2分)或邻二甲苯只有一种结构(2分)或实验测定碳原子之间的化学键键长、键角、键能完全相同(2分)(2)还原反应(2分)酰胺基或酰胺键(2分)COOH(3)(2分)+NH(2分)(2分)COOHCOCI(3分,每步1分有机物结构简式且条件正确得1分)解析苯为原料合成有机化合物I的具体过程如下图所示NaBHCOCZn/HCHCH COCI(COOHCON1)根据苯分子中C原子采取sp杂化,存在大π键这一结构基础,从而推出苯与酸性高锰酸钾溶液、溴水都不能发生反应或邻二甲苯只有一种结构或实验测定碳原子之间的化学键键长、键角、健能完全相同等客观事实(2)(3)略(4)苯的分子式为CH4,其同分异构体含有3个双键;核磁共振氢谱只显示1个吸收峰;不存在甲基只能存在3个“CH:=”,还有3个C原子,故只能是3个C原子的环状结构。结构简式为(5)根据信息I酰氯中的Cl可以与苯环上的H发生取代反应,根据信息Ⅱ知苯甲酸与SOC12可合成酰氯。综合分析可推出合成路线COOCOCISOCZn/Hg

(15分(1)N(1分)Cu原子增加的电子都分布在3d轨道上,它对外层电子的排斥作用与核电荷增加带(2)来的核对电子的吸引力大致相当,故Ti与Cu原子半径相差不大。(2分)sp、sp2(2分)10(2分)H,OCI(3)(2分)(4)12(2分)6(2分)4.2×102(2分)解析(1)第二周期元素第一电离能大于O的元素有:N、F、Ne,三种基态原子核外单电子数分别为3、1、0。故答案为:N。Cu原子增加的电子都分布在3d轨道上,它对外层电子的排斥作用与核电荷增加带来的核对电子的吸引力大致相当,故Ti与Cu原子半径相差不大(2)碳酸乙烯酯中存在C-0)键和C一C键,这两个碳原子采取sp3杂化,C=()键的碳原子采取sp2杂化。C=(键中1个σ键,1个π键,其它化学键为σ键。故1mol碳酸乙烯酯中含有10mola键(3)[Cu(H2O)4]为平面正方形结构,其中的两个H2O被C1取代有两种不同的结构,[Cu(H2O)2(C1)2是非极性分子,说明该分子的结构对称,则其结构式为OH(4)冰晶石(Na1A1F4)晶胞是正四棱柱形状,Na(1)位于侧枝中心和底面中11)位于四个侧面上,AF位于顶点和体心●●Al●FAlF Na(I) Na(l)●AIF冰晶石晶胞结构分析根据结构可知,AIF中,中心原子周围的成键电子总数是12个。若用原子坐标来描述晶胞中所有Na原子的位置,因为晶胞结构有高度对称性,且分数坐标中0和1的意义相同,则需要6组原子坐标。已知晶胞边长为anm,bnm,冰晶石晶体的密度为p=2M2×2104.2×102(a×10210-1×N=ab×10×NAa2bN、g·cm( Na,AlF4的摩尔质量为210g·mol-1)

以上就是2022九年级英语周报新目标人教版第五期答案,更多英语周报答案请关注本网站。






