2022-2022年英语周报高考HNX答案

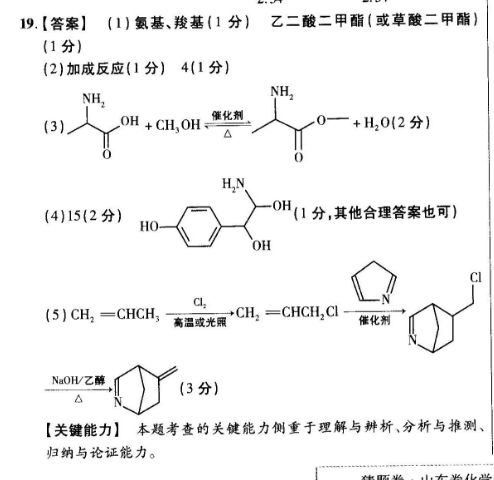

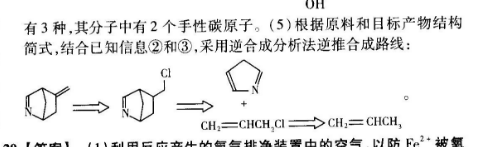
19.【答案】(1)氬基、羧基(1分)乙二酸二甲酯(或草酸二甲酯(1分)(2)加成反应(1分)4(1分)NH)人0H+moH“化机0-+H2O(2分OH(4)15(2分)(1分,其他合理答案也可)HOOH(5)CH2=CHCH2“禽恩或光黑“CH2= CHCH2 C催化剂NaoH(3分)【关键能力】本题考查的关键能力侧重于理解与辨析、分析与推测、归纳与论证能力。图信息转换》NH,分析路线图知,由Y逆推出X为 CH, CHCOOCH,由已知信息①和④知,试剂1为H2 COOCCOOCH2。根据已知信息②并结合P和W的结构简式知,试剂20【解题思路】(1)R含氨基、羧基两种官能团。试剂1的名称是乙二酸二甲酯或草酸二甲酯。(2)W→P的反应是加成反应,生成环状有机物。1个双键是1个不饱和度、1个环是1个不饱和度,故P的不饱和度为4;或根据分子式计算不饱和度,P的分子式为C1H2O4N,不饱和度=NC)+1-NXH)NN=13+1-212=4:(3)R和甲醇在催化剂作用下发生酯化反应。(4)依题意,T含有3个羟基,其中一个为酚羟基。苯环上有一个羟基,另一个取代基有5种结构OHCHCHNH2、HOCH2C一、- NHCHCH2OH、OHNH,HOCH-NHCH2OH、HOCH2NCH2OH。每组取代基有邻、间、对三种位置关系,T有15种结构。一 CHCHNH2与苯环相连的T有3种,其分子中有2个手性碳原子。(5)根据原料和目标产物结构简式,结合已知信息②和③,采用逆合成分析法逆推合成路线:CH=CHCH. CI-CH1= CHCH


【答案】(1)利用反应产生的氢气排净装置中的空气,以防Fe2被氧化(1分)利用反应产生的氢气将B中的FeSO4溶液压入C中与NH4HCO2反应生成FeCO3(1分)(2)Fe2+2HCO=FeCO3↓+CO2↑+H2O(2分)(3)平衡气压,便于液体流下(1分)(4)排尽装置内的空气,防止氧气氧化二价铁和柠檬酸(1分)便于吸收尾气同时防止空气进入F中(1分)(5)促进FeCO3溶解和防止Fe2被氧化(1分)(6)乙醇(1分)75(2分)(7)氨基(一NH2)也被高锰酸钾氧化,导致高锰酸钾溶液用量偏大(1分)【关键能力】本题主要考查利用甘氨酸与FeCO3反应制取甘氨酸亚铁的实验,考查的关键能力侧重于分析与推测、探究与创新能力。【解題思路】(1)实验中先关闭活塞K2,打开活塞K3,滴入稀硫酸(铁粉足量),当反应进行一段时间后才关闭活塞K1,这样操作的目的是利用反应产生的氢气排净装置中的空气,以防Fe2‘被氧化;然后关闭活塞K3,打开活塞K2,目的是利用反应产生的氢气将B中的FeSO4溶液压入C中与NH4HCO3反应生成FeCO3。(2)C中硫酸亚铁和碳酸氢铵反应生成碳酸亚铁,说明Fe2与HCO3电离出的CO3结合生成碳酸亚铁,同时生成的氢离子又和HCO;反应生成二氧化碳和水,所以离子方程式为Fe2+HO=FeCO3↓+CO2↑+H2O。(3)导管a连通滴液漏斗与三颈烧瓶,作用是平衡气压,使液体顺利流下。(4)柠檬酸和亚铁离子具有还原性,易被空气中的氧气氧化,实验前通入氮气,排尽装置内的空气,防止氧气氧化二价铁和柠檬酸;将G装置中导管插入液面以下,可以充分吸收尾气,同时防止空气中的氧气进入F中氧化二价铁和柠檬酸。(5)根据题中的已知信息,柠檬酸具有较强的酸性和还原性,合成过程中加入柠檬酸可促进FeCO3溶解并防止FeCO3被氧化。(6)依題意,甘氨酸亚铁难溶于酒精,加入乙醇可降低其溶解度,使其结晶析出;稀硫酸和铁粉过量,碳酸氢铵的物质的量=0.2L1.0ml,L-1=0.2ml,生成0.lml碳酸亚铁,根据铁原子守恒0.2ml甘1.0ml.L1=0.2mol,生成lmol碳酸亚铁,根据铁原子守恒,02md甘氨酸和0.1ml碳酸亚铁反应理论上生成0.lmol甘氨酸亚铁,质量为204g·mol"×0.1ml=20.4g,所得产品的质量为15.3g,则产率153g×0%=75%。(7)氨基(-NH2)也能被高锰酸钾氧化导致高锰20.4g酸钾溶液用量偏大导致测出的产品纯度大于100%。

以上就是2022-2022年英语周报高考HNX答案,更多英语周报答案请关注本网站。






