20英语周报八年级外答案

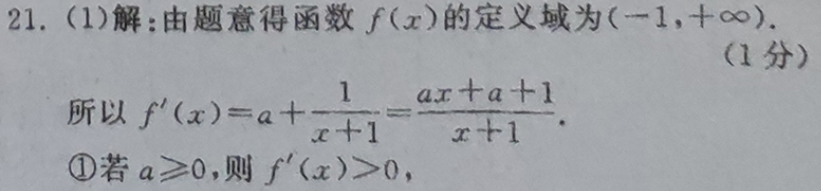


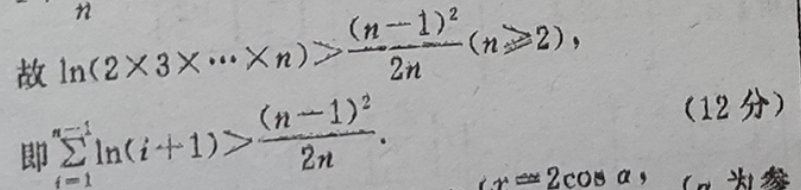
21.(1)解:由题意得函数f(x)的定义域为(-1,+∞)(1分)1 arta+l所以f(x)=a+x+1x+1①若a≥0,则f(x)>0,所以f(x)在区间(-1,+∞)上单调递增;(3分)ai②若a<0,则f(x)=x+1令f(x)>0,得-1

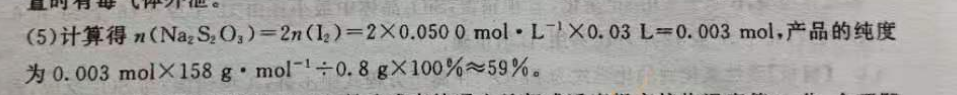
17.(12分)(1)分液漏斗(1分)水浴加热(1分)(2)h-g-d-c-b-a-(-c(2分)(3)2S2+CO3+4SO2-3S2O3+CO2(2分)(4)产生SO2气体的速度过快(过量)或溶液呈酸性使Na2S2O3分解(2分)将残留在装置内的SO2赶出并吸收,防止污染(2分,答案合理即可)(5)59%(2分)【解析】(1)盛放70%硫酸的仪器名称是分液漏斗,装置D采用的加热方式为水浴加热。(2)根据实验装置和目的分析,检验气体产物时,应先检验是否有H2S(连接装置B),再吸收SO2(连接装置A),排除于扰后检验CO2(连接装置C),顺气流方向均为“长进短出”,正确的仪器连接顺序为(i)j-h-g-d-c-b-a-f(e)。(3)根据现象分析可知气体产物为CO2,装置D中发生总反应的离子方程式为2s2+CO+4SO2=35203-+CO(4)装置D中存在反应2S2+3502=2S03+3s↓,出现大量淡黄色固体可能的原因是SO2过量,此时应放慢滴加70%硫酸的速度,让反应充分发生。同时应在反应完毕后,及时停止反应,避免继续通入过量SO2,以免发生反应:S2O3+SO2+H2O=S++2HSO3拆卸装置前打开i处弹簧夹,通入N2,赶出装置中的SO2,使其全部被吸收,可避免拆卸装置时有毒气体外泄。(5)计算得n(Na2S2O3)=2n(2)=2×0.0500mol·Lh×0.03L=0.003mol,产品的纯度为0.003mol×158g·mol1÷0.8g×100%≈59%。

以上就是20英语周报八年级外答案,更多英语周报答案请关注本网站。






