

28.(1)2O2光302(1分)(2)①La2O3(s)+2C0(g)=1a20s)+2CO2(g)△H=+31k·mol②C(各2分)(3)①
K(B)=K(C):>(各1②,9(2分)(4)>(2分)(5)①2H2O+2e=H2↑+2OH(1分②8:3(2分)解析:(1)由反应机理可知,臭氧在光的作用下分解生成氧气和氧原子氧原子与一氧化氮反应生成二氧化氮二氧化氮分子间反应生成一氧化氮和氧气,总反应的化学方程式为20WQ(2)①根据总反应与分步反应的关系可知,总反应一反应I=反应Ⅱ,则反应Ⅱ的热化学方程式为Ia2O3(s)2CO(g)La2O(s)+2CO2(g)△H=+31kJ·mol-l。②判断图像正确与否主要看三个方面反应1和Ⅱ的先后顺序,因为La2O为催化剂,所以先发生反应Ⅱ是否符合总反应以及反应!和的放吸热特点;根据反应速率公式可知反应的速率慢即活化能大,C项正确。(3)①由图可知,温度升高NO2的转化率降低,故该反应为放热反应,温度越高,平衡常数越小A、B、C三点温度高低为T(A)
K(B)=K(C);300℃、P2条件下,E点未达到平衡,且此时NO2的转化率小于平衡时NO2的转化率,则E点的vE>0.5②根据三段式法计算平衡时各物质的分压分别为pa2=.P2,a2=4,52,=15,例O=4,5,×故Kpn2×x24p2(4)由题给数据可知,温度为T时,c(NO2)=0;2mo·L-1、c(NO)=0.4mol·L-1,c(O2)0.2mol·L-1,平衡常数K=0.42×0.2/0.22=0.8;达到平衡状态时v=,则有k正c2(NO2)=k证(NO)·c(O2);当温度变为T2,达到平衡状态时同样有k/k=2(NO)·c(O2)/2(NO2),此时k正/k逆=c2(NO)·c(O2)/(2(NO2)=1>0.8,说明改变温度后平衡正向移动,由于该反应的△H>0,所以(5)①根据装置图,a极为阴极,电极反应式为2H2O+2c—H2↑+2OH,b极为阳极,NO气体发生氧化反应生成硝酸和亚硝酸。②根据原子守恒:n(NO)+n(NO2)=3mol+0.1mol-0.2mol·L-1×10L=1.1mol,根据电子守恒:0.1mol×1+[n(NO)-0.1mo×3+n(NO2)×1=2.4L·m21×2.解得,nNOD8m00.3 mol, V(NO): V(NO2)=n(NO): n(NO2)=0. 8 mol 0 3 mol=8: 3.


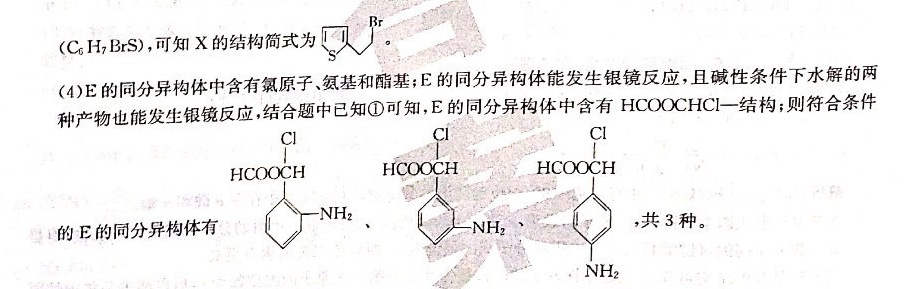

36.[化学——有机化学基础(1)氮气,光照;氨基氯原子羧基(各1分)(2)取代反应(或酯化反应)(1分)人(2分CHIO(2分)J90℃+CH-CH2(3)(4)3, HCOO--CHCHNH2(各2分)7市#12页)【20NHNHCHCI2CH--CNCHCOOHCHONaCN(5)CH2 OH NaOH、H2ONH ClCH,OHCHOHCH, OH浓H2O1HEO-CH2 -CH-ChOH(4分)NH2解析:由B的分子式可知,A→B发生了氯代反应,结合信息③可知C中含一CHO,D中含一NH2和CN结合D的分子式CHN2C)以及E的结构简式逆推出D的结构简式为CHCN,C的结构CHO。反应①为A在光照下与Cl2发生侧链上的取代反应;根据反应⑤的条件可知E简式为〔NH2F为酯化反应,故F的结构简式为COO,对比F和G的结构简式,结合X的分子式cHBS),可知X的结构简式为(4)E的同分异构体中含有氣原子、氨基和酯基;E的同分异构体能发生银镜反应,且碱性条件下水解的两种产物也能发生银镜反应,结合题中已知①可知,E的同分异构体中含有 HCOOCHC-结构;则符合条件HCOOCHHCOOCHHCOOCH的E的同分异构体有,共3种NHHEO→CH2CH-C]OH(5)可以采用逆推法进行分析,要想合成则必须制得单体NHCHCOOH与原料相比,应该引入氨基和羧基,结合题中已知③的反应可知,应该将现原料转化为CH2OHCHOCHCIzCH2OH,结合图中B—C的反应可知,应使OH发生水解反应

以上就是2022英语周报高考第七期答案,更多英语周报答案请关注本网站。














